Kimyasal Tepkimeler

Kimyasal Tepkimeler konusu 8. Sınıf 4. Ünitenin üçüncü konusudur.
F.8.4.3. Kimyasal Tepkimeler
Önerilen Süre: 3 ders saati
Konu / Kavramlar: Kimyasal tepkimelerin oluşumu, kütlenin korunumu
Kazanımlar
F.8.4.3.1. Bileşiklerin kimyasal tepkime sonucunda oluştuğunu bilir.
Kimyasal Tepkimeler
- Maddenin yapısında fiziksel ve kimyasal değişmeler meydana gelir.
- Fiziksel değişmeler sadece dış görünümde meydana gelirken, kimyasal değişmeler maddenin iç yapısında meydana gelir.
- Kimyasal değişim, kimyasal tepkimelerle meydana gelir.
- Demirin paslanması, kağıdın yanması, elmanın çürümesi, ekmeğin küflenmesi kimyasal değişimdir. Bu olaylar kimyasal tepkimelerle oluşur.
- Maddelerin kimyasal değişime uğrayarak yeni maddeler oluşturmasına kimyasal tepkime denir.
Kimyasal Tepkimelerin Özellikleri
• Madde özelliklerini kaybeder yeni madde oluşur.
• Kimyasal özellikler değişir.
• Atomlar arasındaki kimyasal bağlar kopar.
• Farklı atomlarla yeni bağlar oluşur.
• Kimyasal tepkimeye giren atomların türü ve sayısı değişmez.
• Kimyasal tepkimeye giren maddenin kütlesi ile ürünleri kütleleri eşittir.
• Girenlerin ve ürünlerin molekül sayısı ve hacimleri korunmayabilir.
Kimyasal Tepkimelerin Yazılması
Kimyasal tepkimeler yazılırken kimyasal denklem şeklinde gösterilir.
Tepkimeye (Reaksiyona) girenler sol tarafa, ürünler ise sağ tarafa yazılır.
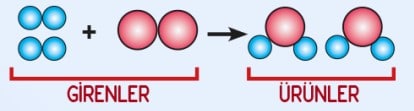
• Tepkimeye girenler ve ürünler birden fazla ise aralarına + işareti konulur.
• Girenler ve ürünler arasına → işareti konulur.
Kimyasal Tepkimelerde Kütlenin Korunumu
- Bir kimyasal tepkimede var olan madde yok olmaz, yoktan da madde var edilemez.
- Madde içerisindeki atomlar arasındaki bağlar kopar ve yeni bağlar oluşur. Bu nedenle yeni maddeler meydana gelir. Atomların sayısı ve türü değişmemektedir.
- Kimyasal tepkimeye giren maddelerin toplam kütlesi ile tepkimeden çıkan maddelerin toplam kütleleri birbirine eşittir. Buna kütlenin korunumu kanunu denir.
Örnek: 16 gram oksijen ile miktarı bilinmeyen karbon tepkimeye girerek, 22 gram karbondioksit oluşuyor. Buna göre tepkimeye giren karbon miktarı kaç gramdır.
CEVAP:
Oksijen + Karbon -> Karbondioksit
16 + ? -> 22
16 + ? =22 => 22-16=6gr , tepkimede 6 gram karbon kullanılmıştır.
Kimyasal Tepkimede Korunanlar
1. Atom Cinsi
2. Atam Sayısı
3. Kütle
Kimyasal Tepkimede Korunmayabilenler
1. Molekül sayısı korunmayabilir.
Kimyasal Tepkimelerin Grafiği
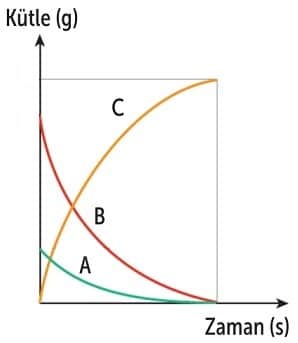
A + B → C
Kimyasal Tepkime Grafiği
• Kimyasal tepkimeye giren maddelerin kütlesi azalır, ürünlerin kütlesi artar.